近年来�,纳米**在癌症**方面受到了广泛关注�。将**高效输送到细胞内靶点是纳米**研发的中心法则,但细胞外靶点在癌症**中同样重要���,分布于细胞外的纳米**对疗效的贡献却远远未被理解�����。
定量纳米**的细胞内外分布是考察其**贡献的前提条件�����,由于复杂的肿瘤微环境�����,蓄积于肿瘤部位的纳米**只有一小部分可以被肿瘤细胞内吞�,其他都被阻滞于细胞外区域。然而���,常规的定量和成像方法只能提供纳米**的宏观组织分布�����,而不能提供其在细胞内和细胞外分布的详细信息���。因此,定量纳米**的细胞内外分布�����,并进一步考察它们的**贡献仍然是一个巨大的挑战���。
北京大学药学院天然**及仿生**国家重点实验室汪贻广团队在 Nature Communications 在线发表了题为:Dissecting extracellular and intracellular distribution of nanoparticles and their contribution to therapeutic response by monochromatic ratiometric imaging(单色比率成像技术解析纳米**的细胞内外分布及其对**效应的贡献)的研究论文�����。

汪贻广团队基于课题组已有的pH超敏感(Ultra-pH-sensitive, UPS)纳米技术平台����,开发了一种pH/光双重响应型的单色比率成像纳米粒(MRIN)��,其可通过响应于细胞内的酸性pH和近红外光依次打开细胞内和细胞外的荧光信号,实现对纳米**细胞内外分布的精准解析�����。通过MRIN纳米技术���,纳米粒在不同肿瘤模型中的细胞外和细胞内分布被准确定量,二者占比分别为65%-80%和20%-35%����。
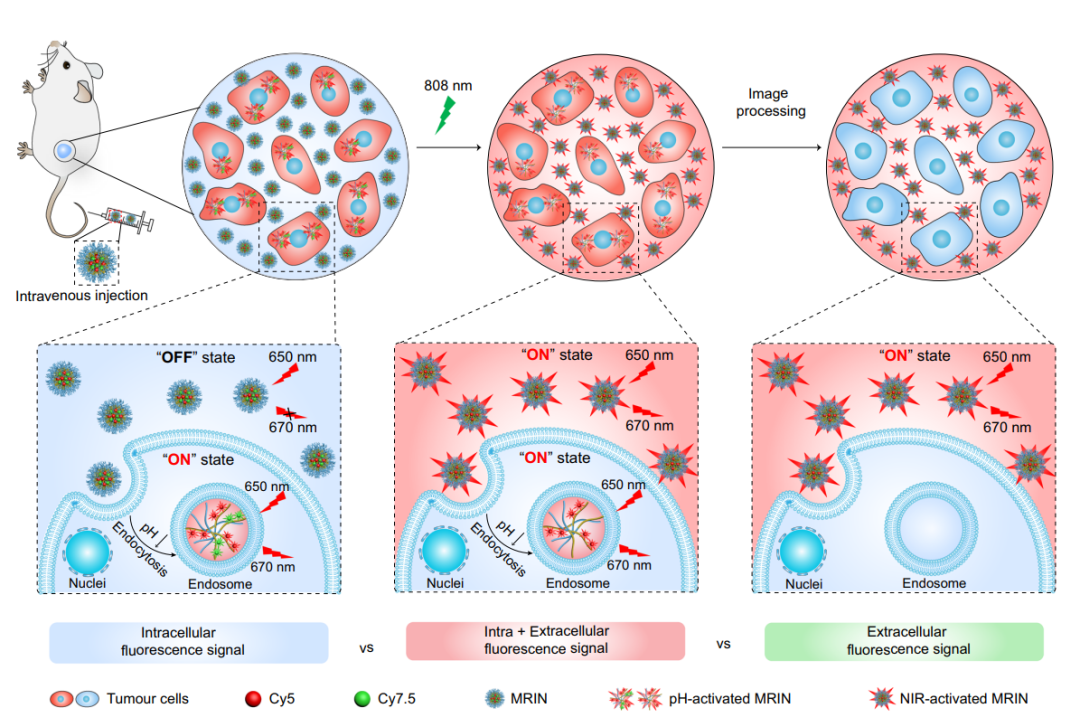
采用该项技术,汪贻广团队成功解析了细胞外分布的纳米光敏剂对肿瘤**的贡献����。结果显示:与单纯细胞内光动力效应相比,细胞内外联合光动力疗法通过破坏肿瘤细胞外基质和促进肿瘤细胞失巢凋亡等机制显著抑制了肿瘤生长和转移����,使肿瘤**效应得到*大化。该项研究为**量化纳米**的微观分布和设计多功能化纳米**提供了新策略���。